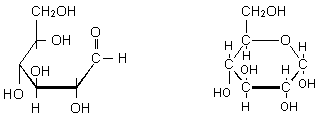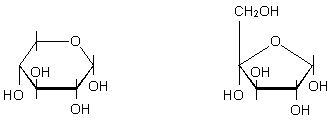1. Grundlagen
Kohlenhydrathaltige Nahrungsmittel sind,
neben den Zuckern, Getreide und alle Getreideprodukte, Hülsenfrüchte,
Kartoffeln, Gemüse und Obst. Kohlenhydrate sind eine wesentliche
Energiequelle des Organismus. Der Aufbau der Kohlenhydrate in den
Pflanzen erfolgt über die Photosynthese, bei der aus CO2,
Wasser und Licht unter Mitwirkung von Chlorophyll Glucose aufgebaut
wird.
Die Kohlenhydrate Zucker, Stärke,
Glykogen, Dextrine und Zellulose sind aus den Elementen Kohlenstoff (C),
Wasserstoff (H) und Sauerstoff (O) aufgebaut. Die Beobachtung, dass
dabei die Elemente C, H und O im Verhältnis 1:2:1 auftreten, was sich in
der Summenformel als (CH2O)n darstellen lässt, hat zur
Bezeichnung Kohlenhydrate, d.h. Hydrate des Kohlenstoffs geführt. Obwohl
heute auch Verbindungen zu den Kohlenhydraten gezählt werden, welche
dieser Bedingung nicht genügen, und zudem Substanzen bekannt sind,
welche zwar den Bedingungen genügen, aber keine Kohlenhydrate sind, wie
beispielsweise die Essigsäure (C2H4O2)
oder die Milchsäure (C3H6O3), wurde die
Bezeichnung beibehalten.
Heute werden Kohlenhydrate definiert als
Aldehyde oder Ketone mit zwei oder mehr Hydroxy-Gruppen.
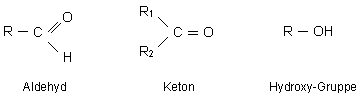
Abb. 1: Aldehyde oder Ketone und
Hydroxy-Gruppen bilden zusammen mit einem Kohlenstoffskelett die
Kohlenhydrate.
Kohlenhydrate mit einem Aldehyd werden
als Aldosen, Kohlenhydrate mit einem Keton als Ketosen bezeichnet.
Kohlenhydrate entstehen aus Polyalkoholen
(= Alkohole mit mehreren OH-Gruppen) dadurch, dass eine Hydroxy-Gruppe
zu einer Carbonyl-Gruppe dehydriert wird, was sich am einfachsten am
Glycerin (Glycerol) zeigen lässt:
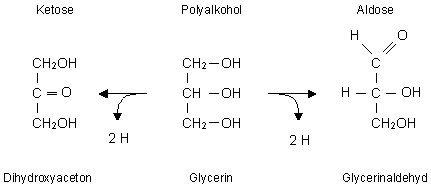
Abb. 2: Bildung der beiden einfachen
Zucker Dihydroxyaceton (Ketose) und Glycerinaldehyd (Aldose) aus dem
Polyalkohol Glycerin (Glycerol) durch Abgabe von 2 Wasserstoffatomen.
Bei den Aldosen ist die Carbonylgruppe
(C=O) am Anfang der Kohlenstoffkette (C1-Atom), bei den Ketosen
innerhalb der Kohlenstoffkette (in der Regel am C2-Atom).
Entsprechend der Anzahl C-Atome in der
Kohlenstoffkette werden Zucker unterteilt in:
|
Anzahl C-Atome |
Bezeichnung |
|
3 |
Triose |
|
4 |
Tetrose |
|
5 |
Pentose |
|
6 |
Hexose |
|
7 |
Heptose |
Die einfachsten Zucker sind demnach
Triosen mit 3 C-Atomen, d.h. sowohl Glycerinaldehyd (Aldose) wie auch
Dihydroxyaceton (Ketose) sind Triosen.
Die in der Nahrung vorkommenden einfachen
Zucker sind vorwiegend Hexosen. Ribose und Desoxyribose in der
Erbsubstanz (Nucleinsäuren) gehören zu den Pentosen.
Nummerierung der
C-Atome
Die Kohlenstoffatome des Kohlenhydratgerüstes werden numeriert. Dabei
beginnt man bei demjenigen C-Atom, welches der Aldehyd-Gruppe bzw. der
Keton-Gruppe am nächsten ist.
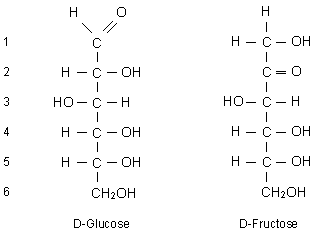
Abb.3: Nummerierung der
Kohlenstoffatome bei Kohlenhydraten.
|
Chiralität: D-
und L-Formen |
|
Aldosen mit drei oder mehr C-Atomen und
Ketosen mit vier oder mehr C-Atomen enthalten sogenannte asymmetrische
Zentren, d.h. sie besitzen Kohlenstoffatome mit 4 verschiedenen
Substituenten.
Je nach dem, ob die Hydroxy-Gruppe am
zweitletzten C-Atom nach rechts oder links schaut, unterscheidet man
zwischen D- und L-Formen. Moleküle, die sich in dieser Art
spiegelbildlich verhalten, werden als Enantiomere oder Stereoisomere
bezeichnet.
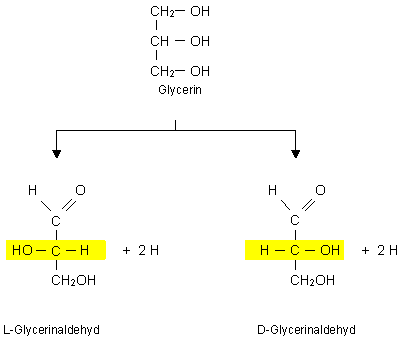
Abb. 4: Entsprechend der Stellung der
OH-Gruppe am "zweitletzten" C-Atom unterscheidet man zwischen D- und
L-Glycerinaldehyd.
Enantiomere besitzen den gleichen Namen,
allerdings mit unterschiedlichem Präfix L oder D. In der Natur
dominieren bei den Kohlenhydraten die D-Formen.
Die Zahl der möglichen Aldosen wächst mit
jedem C-Atom um den Faktor 2. Ausgangspunkt sind bei den Aldosen das D-
und das L-Glycerinaldehyd. Die folgende Abbildung zeigt die möglichen
Aldosen, wenn man vom D-Glycerinaldehyd ausgehend Kohlenstoffatome in
die C-Kette einfügt.
Mögliche D-Aldosen mit 3 bis 6 C-Atomen,
ausgehend vom D-Glycerinaldehyd. Alle hier gezeichneten Aldosen weisen
am vorletzten C-Atom die gleiche Konfiguration auf.
In der gleichen Art lässt sich ein Schema entwickeln, welches auf dem
L-Glycerinaldehyd basiert.
|
Die Ringbildung
der Monosaccharide |
|
In Lösung sind Zucker grösstenteils nicht
in Kettenform vorhanden, sondern bilden durch kovalente Bindung der
Carbonyl-Gruppe mit einer Hydroxy-Gruppe innerhalb der Kohlenstoffkette
zyklische Strukturen.
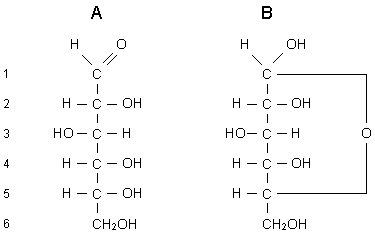
Abb. 5: Ringbildung der Glucose
A: Glucose in Kettendarstellung
B: der Sauerstoff der Carbonylgruppe ist mit dem C5-Atom
verbunden
Bewährt hat sich die Darstellung nach
Haworth:
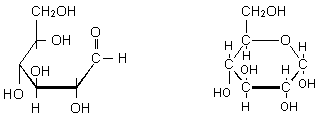
Abb. 6: Darstellung des Ringschlusses
bei der Glucose nach Haworth.
Bei der üblichen Darstellung werden die
Kohlenstoff- und und die Wasserstoffatome innerhalb des Ringes werden
nicht geschrieben:
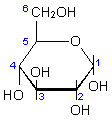
Abb.7: Die übliche Darstellung der
Glucose. In blau die Nummer des jeweiligen C-Atoms.
Die Ringbildung ist möglich für Zucker,
bei denen am Kohlenstoffatom mit der Carbonyl-Gruppe eine Kette von 3
oder mehr C-Atomen hängt.
Die
a-
und b-Konfiguration
Bei der Ringbildung entsteht ein neues asymmetrisches C-Atom. Schaut die
Hydroxygruppe am C1-Atom nach unten, so spricht man von einer
a-Konfiguration,
andernfalls von einer b-Konfiguration.
Die beiden Konfigurationen werden als Anomere bezeichnet.
a- und
b-Konfiguration
gehen leicht ineinander über (Mutarotation).
Pyranosen und
Furanosen
Reagiert bei der Ringbildung von Aldohexosen die OH-Gruppe des C5-Atoms
mit dem C1-Atom, so entsteht ein 6er-Ring, bestehend aus 5 Kohlenstoff-
und einem Sauerstoffatom. Chemisch wird dieser Ring als Pyran
bezeichnet, folglich heissen alle Zucker mit diesem 6er-Ring Pyranosen.
Es kann aber auch die OH-Gruppe am
C4-Atom mit dem Kohlenstoffatom C1 reagieren. Dabei entsteht ein 5er
Ring; diese Kohlenhydrate werden als Furanosen bezeichnet.
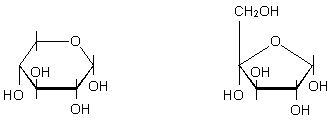
Abb. 8: Pyranose (links) und Furanose
(rechts).
|
Unterteilung der
Kohlenhydrate |
|
Unterteilung
aufgrund der Molekülgrösse
Die Kohlenhydrate lassen sich unterteilen in
- Monosaccharide,
- Disaccharide (2 Monosaccharide)
- Oligosaccharide (3-10 Monosaccharide)
und
- Polysaccharide.
Unterteilung
aufgrund der Funktion
Kohlenhydrate kommen in Form der Monosaccharide und Disaccharide als
einzelne, kleine Moleküle vor. Diese können sich aber zu grösseren
Einheiten zusammenschliessen, welche dann als Speicherform dienen oder
aber strukturelle Aufgaben übernehmen. Zudem wirken Kohlenhydrate als
Signalstoffe.
- Nährstoffe und Reservestoffe
- Glucose
- Glycogen
- Stärke
- Bau- und Gerüststoffe
- Cellulose
- Chitin
- Signal- und Informationsträger
- Glycoproteine: Proteine mit einem Kohlenhydratanteil
- Bestandteile der Erbsubstanz
- Desoxyribose in der DNS (Desoxyribonucleinsäure, DNA)
- Ribose in der RNS (Ribonucleinsäure, RNA).
2. Monosaccharide
|
Einteilung der Monosaccharide |
|
Monosaccharide sind die kleinsten
Einheiten der Kohlenhydrate. Sie sind durch Säuren nicht
spaltbar. Zu den Monosacchariden zählen die einfachen Zucker
sowie deren Derivate.
Die wichtigsten Vertreter der
einfachen Zucker sind die Hexosen Glucose (Traubenzucker, Glc),
Fructose (Fruchtzucker, Fru) sowie Galactose (Cerebrose, Gal)
und die Pentosen Ribose und Desoxyribose.
Bei den Derivaten werden weitere Gruppen an die einfachen Zucker
gebunden. Wichtige Funktionen nehmen die Aminozucker, die
acetylierten Aminozucker und die sauren Monosaccharide ein.
Aufbau
von Glucose, Galactose und Fructose
Diese einfachen Zucker bestehen ausschliesslich aus den
Elementen C, O und H.
 |
 |
 |
|
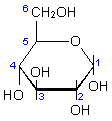
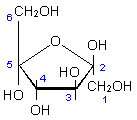
a-D-Glucose |
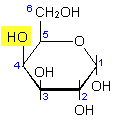
a-D-Galactose |
b-D-Fructose |
Abb. 1: Monosaccharide:
Hexosen
Die beiden Aldosen Glucose und Galactose im Vergleich mit der
Ketose Fructose.
Ribose
und Desoxyribose
 |
 |
|
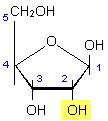
b-D-Ribose |
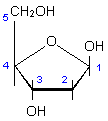
b-D-Desoxyribose |
Abb. 2: Monosaccharide:
Pentosen. Ribose und Desoxyribose
Desoxyribose kommt in der DNA (=
DNS, Desoxyribonucleinsäure), Ribose in der RNA (= RNS,
Ribonucleinsäure) vor.
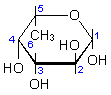
Fucose
Fucose (Fuc, 6-Desoxy-L-Galactose) ist ein Desoxyzucker (C6H12O5),
der als Bestandteil von Oligosacchariden der Frauenmilch, von
Glycoproteinen der Blutgruppen und in Meeralgen vorkommt. Fucose
ist einer der wenigen Zucker, die in der L-Form vorliegen.
 |
|
a-L-Fucose |
Abb.3: Fucose
|
Derivate
der einfachen Zucker |
|
Aminozucker und acetylierte Aminozucker
 |
|
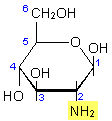
b-D-Glucosamin |
Abb. 4: Beim
b-D-Glucosamin
ist die OH-Gruppe des C2-Atoms durch eine
Amino-Gruppe ersetzt worden.
Durch Bindung von Essigsäure an
die Aminogruppe des Aminozuckers entstehen acetylierte
Aminozucker.
|
|
 |
 |
| |
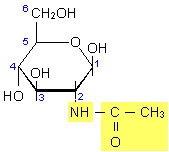
b-N-Acetyl-D-Glucosamin
(GlcNAc) |
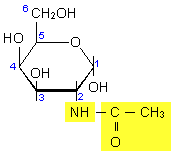
b-N-Acetyl-D-Galactosamin
(GlcNAc) |
Abb. 5: GlcNAc leitet sich von
der Glucose, GalNAc von der Galactose ab.
Galactosamin ist ein häufiger
Bestandteil von Glycoproteinen.
Saure
Monosaccharide
Eine Oxydation ist nur an den Enden der Zuckerkette möglich,
also bei der Glucose am C1- und C6-Atom.
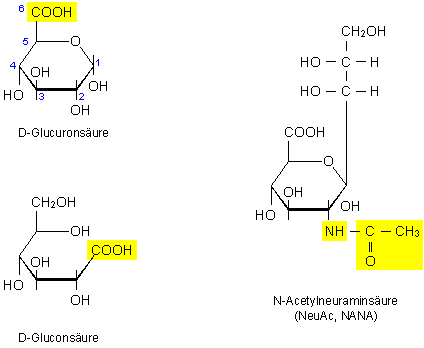
Abb. 6: Saure Monosaccharide
Die Glucuronsäure hat eine
wichtige Funktion in der Leber bei der Entgiftung, so
beispielsweise auch bei der Ausscheidung des Bilirubins durch
die Galle.
Gluconsäure ist als Phosphat ein
Zwischenprodukt im Pentosephosphatzyklus.
Eine zentrale Stellung im
Stoffwechsel nehmen die Verbindungen der Monosaccharide,
insbesondere der Glucose und Fructose, mit Phosphorsäure ein.
Die Phosphat-Gruppe kann dabei vom C1-Atom und/oder
vom C6-Atom gebunden werden.
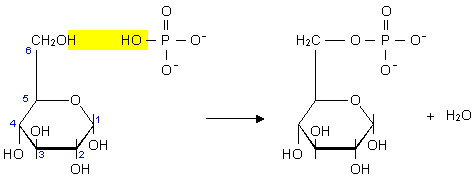
Abb. 7: Glucose-6-Phosphat
Umwandlung von Monosacchariden
- Epimerisierung: Umkehr der
sterischen Anordnung an einem C-Atom
Beispiel: in der Leber wird Galactose in Glucose
umgewandelt.
- Isomerisierung: Umwandlung
von Aldose in Ketose und umgekehrt.
Beispiel: beim Abbau der Glucose durch die Glycolyse wird
Glucose-6-Phosphat in
Fructose-6-Phosphat umgewandelt.
|
3. Disaccharide
|
Disaccharide werden durch
Verknüpfung von zwei Monosacchariden (glycosidische Bindung)
gebildet.
Die wichtigsten Vertreter der
Disaccharide sind:
- Maltose (Malzzucker) =
Glucose + Glucose,
- Lactose (Milchzucker) =
Galactose + Glucose
- Saccharose (Rohrzucker) =
Glucose + Fructose.
Maltose entsteht aus dem
Zusammenschluss zweier Glukosemoleküle, wobei Wasser frei wird.
Die Verknüpfung erfolgt zwischen den Kohlenstoffatomen C1
mit einer Hydroxy-Gruppe in alpha-Stellung und C4 des
zweiten Moleküls, so dass eine
a1,4-glycosidische
Verbindung entsteht: Glucose-a1,4-Glucose.
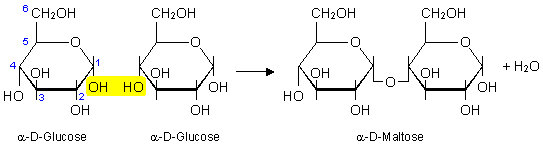
Abb.1: Maltose besteht aus 2
Glucosemolekülen, die mit einer
a-1,4-Bindung
verbunden sind.
Isomaltose
Bei der Isomaltose erfolgt die
Verknüpfung der beiden Glucosemoleküle zwischen dem C1-
und dem C6-Atom.
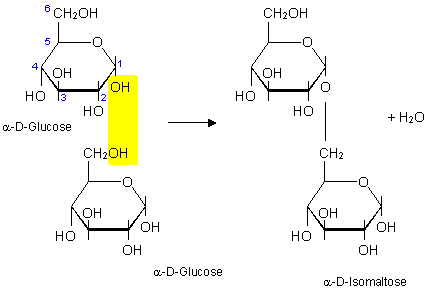
Abb.2: Isomaltose (Glucose-a1,6-Glucose)
Die nur schwach süsse Lactose
(Galactose-b1,4-Glucose)
kommt ausschliesslich in der Milch vor und besteht aus Galactose
und Glucose. Da es sich um eine
b-glycosidische
Verbindung der beiden Monosaccharide handelt, kann das Molekül
auf zwei Arten dargestellt werden:
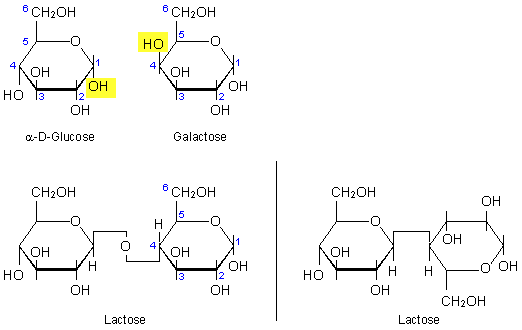
Abb.3: Zwei verschiedene
Darstellungsmöglichkeiten des Lactosemoleküls
Lactose kann durch das Enzym
Lactase gespalten werden.
Saccharose besteht aus Glucose
und Fructose ( Glucose-a1,b2-Fructose).
Im Pflanzenreich ist die
Saccharose die Transportform der Kohlenhydrate und dient auch
als lösliche Kohlenhydrat-Reserve. Da sie sehr süss ist, wird
sie zum Zuckern von Speisen geschätzt. Besonders reich an
Saccharose sind Zuckerrohr und Zuckerrüben.
Durch enzymatische Hydrolyse des
saccharosehaltigen Blüten-Nektars im Verdauungstrakt der Bienen
entsteht der Honig, eine Mischung zwischen Glucose und Fructose.
|
4. Polysaccharide
|
Durch glycosidische Verknüpfung
vieler Monosaccharide entstehen Oligo- bzw. Polysaccharide.
Polysaccharide haben sehr
unterschiedliche Funktionen:
- Glycogen und Stärke sind
Speicherformen der Glucose
- Cellulose ist ein
wesentlicher Bestandteil der Pflanzenzellwände
- Proteoglycane bilden die
Grundsubstanz des Interzellularraums
- Glycoproteine sind zusammen
mit den Glycolipiden wichtige Bestandteile der
Zellmembranen.
Stärke besteht aus unverzweigter
Amylose und aus verzweigtem Amylopectin.
Amylose ist poly-a1,4-Glucose:
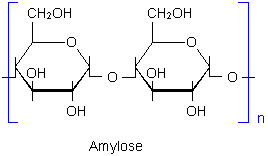
Abb.1: Die in der Stärke
vorkommenden Amylose besteht aus linearen Ketten von a1-4
verknüpften Glucosemolekülen.
Amylopectin ist poly-a1,4-a1,6-Glucose.
durch die Verbindung zwischen den C1- und C6-Atomen entstehen
Verzweigungen.
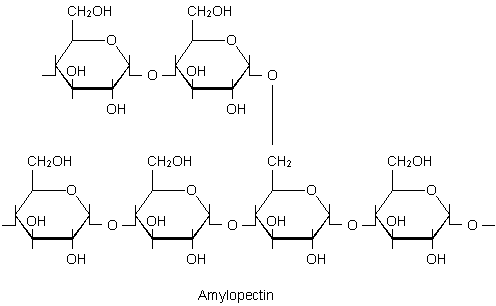
Abb.2: Amylopectin
Im Mittel verzweigt sich die
Kette jeweils nach 25 Glucosemolekülen.
Glykogen ist eine verzweigte
Kette, aufgebaut aus bis zu 100’000 Glucosemolekülen. Glykogen
ist die Kohlenhydratreserve des Menschen und wird vorallem in
Leber und Muskulatur gespeichert.
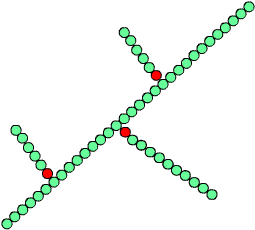
Abb.3: Schematische
Darstellung eines Glycogenmoleküls. Durch
a1,4-glycosidische
Bindungen entstehen lineare Ketten,
a1,6-glycosidische
Bindungen führen zu Verzweigungen.
Glycogen ist wesentlich stärker
verzweigt als Amylopectin, nach jedem 8. bis 12. Glucosemolekül
tritt eine Verzweigung auf.
Cellulose bildet ein lineares,
unverzweigtes Molekül aus b1-4
verknüpften Glucosemolekülen.
Cellulosemoleküle können mehr als 10’000 Glucosereste enthalten
und eine Länge von 6-8 mm erreichen. Sie sind mechanisch stabil,
wasserunlöslich und gegenüber chemischer und enzymatischer
Hydrolyse sehr widerstandsfähig. Im menschlichen Darmtrakt kann
Cellulose nicht abgebaut werden.
Pflanzliche Zellwände bestehen
fast zur Hälfte aus Cellulose, bei Baumwollfasern liegt der
Celluloseanteil sogar bei 98%.
Die sauren Mucopolysaccharide,
auch als Glykosaminglykane bezeichnet, bestehen aus
Disaccharideinheiten, welche 1-4-glykosidisch zu linearen
Polysacchariden verbunden sind.
Diese Disaccharideinheiten
bestehen aus Glucuronsäure und Aminozuckern, die
1-3-glykosidisch verbunden sind. Diese Einheiten können zudem
noch sulfatiert oder acetyliert sein.
Hyaluronsäure
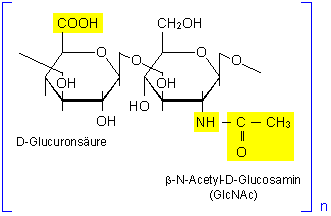
Abb.4: Hyaluronsäure:
Glucuronsäure-b-1-3-N-Acetyl-Glucosamin.
Hyaluronsäure ist ein wichtiger
Bestandteil verschiedener Gewebe:
- Bindegewebsgrundsubstanz
- Synovialflüssigkeit
- Glaskörper des Auges
- Haut
- Knorpel
Hyaluronsäure ist in der Lage
Wasser bis zum 10’000-fachen des Eigenvolumens gelartig zu
fixieren. So enthält der Glaskörper des Auges ca. 1%
Hyaluronsäure und 98% Wasser.
Hyaluronidasen können Hyalinsäure
rasch spalten, wodurch Fremdsubstanzen sowie Bakterien leicht in
das Gewebe eindringen können.
Chondroitinsulfat C
(Glucuronsäure-N-Acetyl-Sulfo-Galactosamin)
Chondroitinsulfat kommt vorallem vor in Bindegewebe, Knochen und
Haut.
Keratansulfat
(D-Galactose-N-Acetyl-Glucosamin-6-sulfat)
Keratansulfat spielt eine Rolle als Bestandteil der Kornea und
des Knorpels.
Werden Mucopolysaccharide im
Gewebe kovalent über die Aminosäuren Serin oder Threonin an
Proteine geknüpft, entstehen Proteoglykane. Sie sind durch einen
grossen Glykananteil (=Polysaccharidanteil) von 80-94% und einen
kleinen Proteinanteil (6-20%) gekennzeichnet.
Proteoglykane sind am Aufbau der extrazellulären
Bindegewebsmatrix beteiligt und besitzen ein hohes
Wasserbindungsvermögen.
Anmerkung: im Gegensatz dazu bestehen Glykoproteine
vorwiegend aus Proteinen, wobei der Kohlenhydratanteil in Form
von Oligosaccharidketten vorliegt. Glycoproteine findet man
vorallem an der Aussenseite von Zellmembranen als
"Erkennungsmoleküle".
|
|